Митохондрии - органеллы энергообеспечения метаболических процесов в клетке. Размеры их варьируют от 0,5 до 5-7 мкм, количество в клетке составляет от 50 до 1000 и более. В гиалоплазме митохондрии распределены обычно диффузно, однако в специализированных клетках сосредоточены в тех участках, где имеется наибольшая потребность в энергии. Например, в мышечных клетках и симпластах большие количества митохондрий сосредоточены вдоль рабочих элементов - сократительных фибрилл. В клетках, функции которых сопряжены с особо высокими энергозатратами, митохондрии образуют множественные контакты, объединяясь в сеть, или кластеры (кардиомиоциты и симпласты скелетной мышечной ткани). В клетке митохондрии выполняют функцию дыхания. Клеточное дыхание - это последовательность реакций, с помощью которых клетка использует энергию связей органических молекул для синтеза макроэргических соединений типа АТФ. Образующиеся внутри митохондрии молекулы АТФ переносятся наружу, обмениваясь на молекулы АДФ, находящиеся вне митохондрии. В живой клетке митохондрии могут передвигаться с помощью элементов цитоскелета. На ультрамикроскопическом уровне стенка митохондрии состоит из двух мембран - наружной и внутренней. Наружная мембрана имеет относительно ровную поверхность, внутренняя - образует направленные в центр складки, или кристы. Между наружной и внутренней мембранами возникает неширокое (около 15 нм) пространство, которое называется наружной камерой митохондрии; внутренняя мембрана ограничивает внутреннюю камеру. Содержимое наружной и внутренней камер митохондрии различно, и так же, как и сами мембраны, существенно отличается не только по рельефу поверхности, но и по ряду биохимических и функциональных признаков. Наружная мембрана по химическому составу и свойствам близка к другим внутриклеточным мембранам и плазмолемме.
Ее характеризует высокая проницаемость, благодаря наличию гидрофильных белковых каналов. Эта мембрана имеет в своем составе рецепторные комплексы, распознающие и связывающие вещества, поступающие в митохондрию. Ферментный спектр наружной мембраны небогат: это ферменты метаболизма жирных кислот, фосфолипидов, липидов и др. Главной функцией наружной мембраны митохондрии является отграничение органеллы от гиалоплазмы и транспорт необходимых для осуществления клеточного дыхания субстратов. Внутренняя мембрана митохондрий в большинстве клеток тканей различных органов формирует кристы в виде пластин (ламеллярные кристы), что значительно увеличивает площадь поверхности внутренней мембраны. В последней 20-25 % всех белковых молекул составляют ферменты дыхательной цепи и окислительного фосфорилирования. В эндокринных клетках надпочечников и половых желез митохондрии участвуют в синтезе стероидных гормонов. В этих клетках митохондрии имеют кристы в виде трубочек (тубул), упорядоченно расположенных в определенном направлении. Поэтому кристы митохондрий в стероидпродуцирующих клетках названных органов именуются тубулярными. Матрикс митохондрии, или содержимое внутренней камеры, представляет собой гелеобразную структуру, содержащую около 50 % белков. Осмиофильные тельца, описанные при электронной микроскопии, - это резервы кальция. Матрикс содержит ферменты цикла лимонной кислоты, катализирующие окисление жирных кислот, синтез рибосом, ферменты, участвующие в синтезе РНК и ДНК. Общее число ферментов превышает 40. Помимо ферментов, матрикс митохондрии содержит митохондриальную ДНК (митДНК) и митохондриальные рибосомы. Молекула митДНК имеет кольцевидную форму. Возможности внутримитохондриального белкового синтеза ограничены - здесь синтезируются транспортные белки митохондриальных мембран и некоторые ферментные белки, участвующие в фосфорилировании АДФ. Все остальные белки митохондрии кодируются ядерной ДНК, и их синтез осуществляется в гиалоплазме, и в дальнейшем они транспортируются в митохондрию. Жизненный цикл митохондрий в клетке короткий, поэтому природа наделила их двойственной системой воспроизводства - помимо деления материнской митохондрии, возможно образование нескольких дочерних органелл путем почкования.
МИТОХОНДРИИ (mitochondria ; греч, mitos нить + chondrion зернышко) - органоиды, присутствующие в цитоплазме клеток животных и растительных организмов. М. принимают участие в процессах дыхания и окислительного фосфорилирования, продуцируют энергию, необходимую для функционирования клетки, представляя, таким образом, ее «силовые станции».
Термин «митохондрии» был предложен в 1894 г. Бендой (С. Benda). В середине 30-х гг. 20 в. удалось впервые выделить М. из клеток печени, что позволило исследовать эти структуры биохим, методами. В 1948 г. Хогебумом (G. Hogeboom) были получены окончательные доказательства того, что М. действительно являются центрами клеточного дыхания. Значительные успехи в изучении этих органоидов были сделаны в 60-70 гг. в связи с применением методов электронной микроскопии и молекулярной биологии.
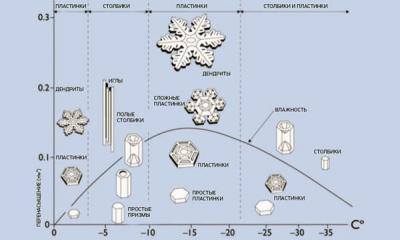
Форма М. варьирует от почти круглых до сильно вытянутых, имеющих вид нитей (рис. 1), Размер их колеблется от 0,1 до 7 мкм. Количество М. в клетке зависит от типа ткани и функционального состояния организма. Так, в сперматозоидах число М. невелико - ок. 20 (на клетку), в клетках эпителия почечных канальцев млекопитающих их содержится до 300 в каждой, а у гигантской амебы (Chaos chaos) обнаружено 500 000 митохондрий, В одной клетке печени крысы ок. 3000 М., однако в процессе голодания животного число М. может сократиться до 700. Обычно М. распределяются в цитоплазме достаточно равномерно, однако в клетках нек-рых тканей М. могут быть постоянно локализованы в участках, особенно нуждающихся в энергии. Напр., в скелетной мышце М. часто находятся в контакте с контрактильными участками миофибрилл, образуя правильные трехмерные структуры. В сперматозоидах М. образуют спиральный футляр вокруг осевой нити хвоста, что, вероятно, связано с возможностью использовать энергию АТФ, синтезируемую в М., для движений хвоста. В аксонах М. концентрируются вблизи синаптических окончаний, где происходит процесс передачи нервных импульсов, сопровождающийся энергозатратой. В клетках эпителия почечных канальцев М. связаны с выпячиваниями базальной клеточной мембраны. Это вызвано необходимостью постоянного и интенсивного снабжения энергией процесса активного переноса воды и растворенных в ней веществ, протекающего в почках.

Электронно-микроскопически установлено, что М. содержит две мембраны - наружную и внутреннюю. Толщина каждой мембраны ок. 6 нм, расстояние между ними - 6-8 нм. Наружная мембрана гладкая, внутренняя образует сложные выросты (кристы), вдающиеся в полость митохондрии (рис. 2). Внутреннее пространство М. носит название матрикса. Мембраны представляют собой пленку из компактно уложенных молекул белков и липидов, в то время как матрикс подобен гелю и содержит в своем составе растворимые белки, фосфаты и другие хим. соединения. Обычно матрикс выглядит гомогенным, лишь в нек-рых случаях в нем можно обнаружить тонкие нити, трубочки и гранулы, содержащие ионы кальция и магния.
Из особенностей строения внутренней мембраны необходимо отметить наличие в ней сферических частиц ок. 8-10 нм в поперечнике, сидящих на короткой ножке и иногда выступающих в матрикс. Эти частицы были открыты в 1962 г. Фернандес-Мораном (H. Fernandez-Moran). Они состоят из белка, обладающего АТФ-азной активностью, получившего обозначение F1. Белок прикрепляется к внутренней мембране только со стороны, обращенной к матриксу. Частицы F1 располагаются на расстоянии 10 нм друг от друга, а в каждой М. содержится 10 4 -10 5 , таких частиц.
В кристах и внутренних мембранах М. содержится большинство дыхательных ферментов (см.), дыхательные ферменты организованы в компактные ансамбли, распределенные с правильными промежутками в кристах М. на расстоянии 20 нм друг от друга.
М. почти всех типов клеток животных и растений построены по единому принципу, однако возможны отклонения в деталях. Так, кристы могут располагаться не только поперек длинной оси органоида, но и продольно, напр, в М. синаптической зоны аксона. В ряде случаев кристы могут ветвиться. В М. простейших организмов, нек-рых насекомых и в клетках клубочковой зоны надпочечников кристы имеют форму трубочек. Число крист различно; так, в М. клеток печени и половых клеток крист очень мало и они короткие, в то время как матрикс обилен; в М. мышечных клеток кристы многочисленны, а матрикса мало. Существует мнение, что число крист коррелирует с окислительной активностью М.
Во внутренней мембране М. осуществляются параллельно три процесса: окисление субстрата цикла Кребса (см. Трикарбоновых кислот цикл), перенос освободившихся при этом электронов и накопление энергии путем образования макроэргических связей аденозинтрифосфата (см. Аденозинфосфорные кислоты). Основной функцией М. является сопряжение синтеза АТФ (из АДФ и неорганического фосфора) и аэробного процесса окисления (см. Окисление биологическое). Накопленная в молекулах АТФ энергия может трансформироваться в механическую (в мышцах), электрическую (нервная система), осмотическую (почки) и т. д. Процессы аэробного дыхания (см. Окисление биологическое) и сопряженного с ним окислительного фосфорилирования (см.) являются основными функциями М. Кроме того, в наружной мембране М. может происходить окисление жирных к-т, фосфолипидов и нек-рых других соединений.
В 1963 г. Насс и Насс (М. Nass, S. Nass) установили, что в М. содержится ДНК (одна или несколько молекул). Все исследованные до сих пор митохондриальные ДНК из животных клеток состоят из ковалентно замкнутых колец диам. ок. 5 нм. У растений митохондриальная ДНК значительно длиннее и не всегда имеет форму кольца. Митохондриальная ДНК во многих отношениях отличается от ядерной. Репликация ДНК происходит при помощи обычного механизма, однако не совпадает во времени с репликацией ядерной ДНК. Количество генетической информации, заключенной в молекуле митохондриальной ДНК, по-видимому, недостаточно для кодирования всех белков и ферментов, содержащихся в М. Митохондриальные гены кодируют в основном структурные белки мембран и белки, участвующие в морфогенезе митохондрий. М. имеют свои транспортные РНК и синтетазы, содержат все компоненты, необходимые для синтеза белка; их рибосомы меньше цитоплазматических и более похожи на рибосомы бактерий.
Продолжительность жизни М. сравнительно невелика. Так, время обновления половины количества М. составляет для печени 9,6-10,2 сут., для почки - 12,4 сут. Пополнение популяции М. происходит, как правило, из предсуществующих (материнских) М. путем их деления или почкования.
Давно высказывалось предположение, что в процессе эволюции М. возникли, вероятно, путем эндосимбиоза примитивных ядросодержащих клеток с бактериоподобными организмами. Имеется большое число доказательств этому: наличие собственной ДНК, более сходной с ДНК бактерий, чем с ДНК ядра клетки; присутствие в М. рибосом; синтез ДНК-зависимой РНК; чувствительность митохондриальных белков к антибактериальному препарату - хлорамфениколу; сходство с бактериями в реализации дыхательной цепи; морфол., биохим, и физиол, различия между внутренней и наружной мембраной. Согласно симбиотической теории клетка-хозяин рассматривается как анаэробный организм, источником энергии для к-рого является гликолиз (протекающий в цитоплазме). В «симбионте» же реализуется цикл Кребса и дыхательная цепь; он способен к дыханию и окислительному фосфорилированию (см.).
М. являются весьма лабильными внутриклеточными органоидами, раньше других реагирующими на возникновение каких-либо патол, состояний. Возможны изменения числа М. в клетке (вернее, в их популяциях) или изменения их структуры. Напр., при голодании, действии ионизирующего облучения число М. уменьшается. Структурные изменения обычно состоят в набухании всего органоида, просветлении матрикса, разрушении крист, нарушении целостности наружной мембраны.
Набухание сопровождается значительным изменением объема М. В частности, при ишемии миокарда объем М. увеличивается в 10 раз и более. Различают два типа набухания: в одном случае оно связано с изменением осмотического давления внутри клетки, в других случаях - с изменениями клеточного дыхания, сопряженного с ферментативными реакциями и первичными функциональными расстройствами, вызывающими изменения водного обмена. Помимо набухания, может происходить вакуолизация М.
Независимо от причин, вызывающих патол, состояние (гипоксия, гиперфункция, интоксикация), изменения М. довольно стереотипны и неспецифичны.
Наблюдаются такие изменения структуры и функции М., к-рые, по-видимому, становились причиной возникновения болезни. В 1962 г. Луфт (R. Luft) описал случай «митохондриальной болезни». Больному с резко повышенной интенсивностью обмена веществ (при нормальной функции щитовидной железы) была сделана пункция скелетной мышцы и найдено повышенное число М., а также нарушение структуры крист. Дефектные митохондрии в клетках печени наблюдались и при выраженном тиреотоксикозе. Виноград (J. Vinograd) с сотр. (с 1937 по 1969) обнаружил, что у больных с определенными формами лейкемии митохондриальные ДНК из лейкоцитов заметно отличались от нормальных. Они представляли собой открытые кольца или группы сцепленных колец. Частота этих аномальных форм снижалась в результате химиотерапии.
Библиография: Гаузе Г. Г. Митохондриальная ДНК, М., 1977,библиогр.; Д e P о-бертис Э., Новинский В. и С а э с Ф. Биология клетки, пер. с англ., М., 1973; Озернюк Н. Д. Рост и воспроизведение митохондрий, М., 1978, библиогр.; Поликар А. и Бесси М. Элементы патологии клетки, пер. с франц., М., 1970; РудинД. и Уилки Д. Биогенез митохондрий, пер. с англ., М., 1970, библиогр.; Серов В. В. и Пауков В. С. Ультраструктурная патология, М., 1975; С э д ж e р Р. Цитоплазматические гены и органеллы, пер. с англ., М., 1975.
Т. А. Залетаева.
Митохондрии (МТ) – одно из самых интересных мне направлений исследований. Объединение митохондрий с другой клеткой в ходе эндосимбиоза около 1,6 млрд лет назад стало основной всех многоклеточных эукариотов со сложной структурой. Предположительно митохондрии произошли от клеток, напоминающих α-протеобактерии.
Лучшее обзорное исследование последнего времени по митохондриях – работа Вернера Кулбрандта «Структура и функция митохондриальных белковых комплексов мембраны ». Если вы знаете английский язык и интересуетесь устройством этих органелл, то настоятельно рекомендую к прочтению. Эта статья так хороша, что может быть смело главой хорошего учебника по молекулярной биологии. Сначала я хотел перевести всю статью, но это бы заняло непростительно много времени и оторвало бы от других дел. Поэтому ограничусь тезисами и картинками. Периодически разбавляя все своими мыслями.
Митохондрия кодирует сама только 13 белков, не смотря на наличие отдельной от клетки ДНК (мтДНК) и всего «производственного» цикла по транскрипции белков. Изолированная митохондрия какое-то время может сохранять композицию и функционировать.
Рисунок 1. Компоненты мембраны митохондриона. Внешняя мембрана отделяет митохондрию от цитоплазмы. Она окружает внутреннюю мембрану, которая отделяет межмембранное пространство от богатого белками центрального матрикса. Внутреннюю мембрану разделяют на внутреннюю пограничную мембрану и кристы. Две эти части непрерывны в местах крепления крист (cristae junction ). Кристы простираются более или менее глубоко в матрикс и являются основным место митохондриального преобразования энергии. Небольшой протоновый градиент в межмембранном пространстве (pH 7,2-7,4) и матрикс (pH 7,9-8,0) приводят к образованию АТФ АТФ-синтазой в мембранах крист.
Внешняя мембрана пористая и позволяет веществам из цитоплазмы проходить через нее. Внутренняя мембрана плотная, для ее пересечения нужны транспортные белки [Гилберт Линг обоснованно не согласен], непрерывность барьера позволяет иметь внутренней мембране электрохимический потенциал в -180 mV. У матрикса довольно большой pH (7,9-8). Еще раз углублюсь в Линга. Щелочной (выше 7) pH способствует более развернутой конформации белков . Высокий pH нарушает водородные и солевые связи, делая поляризованные CO и NH доступными молекулам воды, там самым усиливая дипольный момент всей внутриклеточной воды и связывая ее. В этом ключе наличие мембраны нужно не для «удержания» протоплазмы внутри клетки (это делают сами белки при высоком pH), а для наличия потенциала.
мтДНК находится в нуклеотидах, которых примерно 1000 на клетку. Белковая плотность матрикса довольна высокая (до 500 мг/мл), что близко к кристаллизованным белкам.
Внутренняя мембрана образует инвагинации, называемые кристами, которые глубоко проникают в матрикс. Кристы определяют третий «отсек» митохондрий – просвет крист (cristae lumen). Мембраны кристы содержат большинство, если не все, полностью «собранные» комплексы цепи переноса электронов и АТФ-синтазы. Просвет кристы содержит большое количество маленького растворимого белкового переносчика электронов (цитохром с). Митохондриальные кристы, таким образом, основное место биологической конверсии энергии во всех не фотосинтетических эукариотах.
С кристами тоже много всего интересного. Оптические свойства кристы влияют на распространение и генерацию света в тканях. Я даже встречал идеи о том, что поверхность крист подобна (предположение) поверхностям топологических изоляторов (подразумевалась суперпроводимость без диссипации заряда).

Рисунок 2. Мембранные белковые комплексы дыхательной цепи. Комплекс I (NADH / убихинон оксидоредуктаза, синий), Комплекс II (сукцинат дегидрогеназа, розовы), Комплекс III (цитохром С редуктаза, оранжевый), Комплекс IV (цитохром С оксидаза, зеленый) и митохондриальная АТФ синтаза (известная как комплекс V , бежевая) работают вместе во время окислительного фосфорилирования, чтобы клетки могли использовать энергию. Комплексы I , III , IV выкачивают протоны вдоль мембраны кристы, создавая протоновый градиент, стимулирующий синтез АТФ.
Теперь немного внимания на комплекс II. Вы помните, что жир (кето) делает упор в метаболизме на FADH2 и комплекс II. Они восстанавливают пару CoQ, в какой-то момент окисленного CoQ не хватает для транспортировки электронов на комплекс III и образует обратный поток электронов на комплекс I с образованием супероксида. При долгом HFLC-питании комплекс I будет обратимо разрушен, при этом это нормальная физиологическая оптимизация.
Еще прошу вас заметить, что комплекс II не выкачивает протоны. Что у нас рассеивает протоновый градиент, нарушает фосфорилирование и стимулирует сжигание жиров на тепло? Правильно, стресс холода. Термогенез связан с метаболизмом через комплекс, который не выкачивает протоны, тем самым не давая дополнительных протонов для АТФ-синтазы. Можно только удивляться как замечательно у нас продуман организм.
Крепления крист и MICOS
Места крепления крист (cristae junctions) – маленькие круглы отверстия примерно 25 нм диаметром. В митохондриях всех организмов есть система MICOS (mitochondria contact site and cristae to outer membrane), сборка из пяти мембранных и одного растворимого белков, прикрепляющих кристы к наружной мембране.
В клетках с повышенной потребностью в энергии, такие как скелетные и сердечные мышцы, кристы плотно заполняют большую часть объема митохондрии. В тканях с меньшими потребностями в энергии, таких как печень и почки, кристы находятся не так плотно по отношению друг к другу. Остается больше места в матрице для биосинтетических ферментов.

Рисунок 3. Томографический объем митохондрии сердца мыши. А) Трехмерный объем митохондрии сердца мыши, снятый cryo-ET. Наружная мембрана (серая) окутывает внутреннюю мембрану (светло-синяя). Внутренняя мембрана плотно наполнена кристами б) Томографический срез объема. Плотно заполненный матрикс, содержащий большую часть митохондриальных белков, выглядит темным на электронном микроскопе. В то время как межмембранное пространство и просветы крист выглядят светлыми из-за низкой концентрации белков.
Димеры АТФ синтазы
Митохондриальная F1-F0 АТФ синтаза является самым заметным белковым комплексом кристы. АТФ синтаза – это древняя наномашина, которая использует электрохимический протновых градиент вокруг внутренней мембраны для создания АФТ посредством вращательного катализа . Протоны, двигающиеся через F0 комплекс мембраны, вращают ротор из 8 (у млекопитающих) или 10 (у дрожжей) с-узлов. Центральный стебель передает крутящий момент c-ротора каталитической головке F1, где АТФ образуется из АДФ и фосфата через последовательность конформационных изменения. Периферийный стебель предотвращает непродуктивное вращение Головы F1 против комплекса F0.
Многие годы считалось, что АТФ синтаза случайным образом располагается на внутренней мембране. Но оказалось, что АТФ синтаза располагается двойными рядами . Причем линейные ряды АТФ синтазы – фундаментальный атрибут всех живых митохондрий.

Рисунок 4. Двойные ряды АТФ синтазы у семи разных видов.
Ряды АТФ синтазы располагаются в основном вдоль хребтов крист. Димеры изгибают липидный бислой и как следствие само-организуются в ряды. Когда у митохондрий дрожжей выбивали узлы e и g АФТ синтазы, то штамм рос на 60% медленней диких собратьев, и потенциал мембран их митохондрий был снижен вдвое. У АФТ синтазы прокариотов недостает нескольких узлов, связанных с димерами, ряды димеров не были найдены у бактерий и архей. Кристы и ряды димеров АФТ синтазы, таким образом, являются адаптацией к большим энергетическим потребностям организма.

Рисунок 5. Структура димера АТФ синтазы митохондрии polymella sp. Вид сбоку на V-образный димер АТФ синтазы.
Комплексы и суперкомплексы дыхательной цепи
Протоновый градиент вокруг внутренней мембраны создается тремя крупными мембранными комплексами, известными как комплекс I, комплекс III и комплекс IV (см. рисунок 2). Комплекс I кормится электронами из NADH, высвобождаемая при передаче электрона энергия выкачивает четыре протона. Комплекс III получает электрон от восстановленного хинола и передает его носителю электронов (цитохрому с), выкачивая в процессе один протон. Комплекс IV получает электрон из цитохрома с и передает его молекулярному кислороду, выкачивая 4 протона за каждую молекулу кислорода, превращенную в воду. Комплекс II не выкачивает протоны, напрямую передавая электроны хинолу. Как перенос электронов из NADH в хинол связан с транслокацией протонов пока не ясно. Комплекс I – крупнее III и IV вместе взятых.

Рисунок 6. Комплекс I митохондрии коровьего сердца. Матриксная часть содержит ряд из восьми железно-серных (Fe-S) кластеров, которые направляют электроны из NADH в хинол на пересечении матрикса и мембраны. Мембранная часть состоит из 78 лопастей, включая выкачивающие протоны молекулы.
Комплексы I, III и IV соединяются в суперкомплексы или респирасомы. У пекарских дрожжей (saccharomyces cerevisiae ) нет комплекса I, их суперкомплексы состоят из III и IV. Роль суперкомплексов пока еще не ясна. Предполагают, что это делает транспорт электронов более эффективным, но прямых доказательств этому пока нет.

Рисунок 7. Суперкомплекс митохондрии коровьего сердца. Обратите внимание на дистанцию между комплексами I и III, который надо проделать хинолу. Стрелки – движения электрона в суперкомплексе.
Основным белком просвета кристы является цитохром с, который переносит электрон из комплекса III в комплекс IV. Если цитохром с высвобождается в цитоплазму клетки, то вызывает апоптоз .

Рисунок 8. Ряды димеров АТФ синтазы задают форму кристам. У хребта кристы АФТ синтаза (желтый) образует слив для протонов (красный), протоновые насосы электронной цепи (зеленый) находятся по обоим сторона рядов димеров. Направляя протоны от источника к АТФ синтазе, кристы работают как протоновые направляющие, позволяющие эффективное производство АТФ. Красные стрелки показывают направление потока протонов.
Реорганизация мембраны во время старения
Старение – фундаментальный и плохо понимаемый процесс всех эукариотов. Исследовали старение митохондрий на грибах Podospora anserina , которые живут всего 18 дней. В нормальной митохондрии кристы проникают глубоко в матрикс. Для этого нужны ряды димеров АТФ синтазы и MICOS комплекс у мест крепления крист. С возрастом кристы начинают все ближе подходить к поверхности мембраны, димеры АФТ синтазы превщаются в мономеры, и все заканчивается высвобождением цитохрома с и клеточной смертью.
Транспорт электронов создает супероксид в комплексах I и III. Это побочный продукт метаболизма. Одновременно необходимый и смертельно опасный. Во время старения деление (fission) начинает превалировать над сращением (fussion). Это не дает поврежденным митохондриям «спастись» путем сращения и ускоряет неизбежное.

Рисунок 9. Изменения морфологии внутренней мембраны и димеров АТФ синтазы во время старения митохондрии.
Как видите, полей для будущих исследований очень много. Я предполагаю стык физики и биологии, где физики будут пытаются объяснить почему такая структура более энергетически эффективна. Тем более публикации по квантовой биологии
В клетках любых живых организмов есть особые органеллы, которые двигаются, функционируют, сливаются между собой и размножаются. Называются они митохондриями или хондриосомами. Подобные структуры содержатся как в клетках простейших организмов, так и в клетках растений и животных. Долгое время при изучении изучались и функции митохондрии, потому что она представляла особый интерес.
Действительно, на клеточном уровне митохондрии выполняют конкретную и весьма важную функцию - образуют энергию в виде аденозинтрифосфата. Это ключевой нуклеотид в обмене организмов и преобразовании его в энергию. АТФ выступает в роли универсального источника энергии, необходимой для протекания любых биохимических процессов в организме. В этом главные функции митохондрии - поддерживать жизнедеятельность на клеточном уровне за счёт формирования АТФ.
Процессы, происходящие в клетках, долгое время представляли особый интерес учёных, потому что это помогало лучше понять структуру и возможности организма. Процесс познания всегда занимает долгое время. Так Карл Ломанн в 1929 году открыл аденозинтрифосфат, а Фриц Липман в 1941 году разобрался в том, что он является основным поставщиком энергии в клетки.
Строение митохондрий
Внешний вид представляет такой же интерес, как и функции митохондрии. Размеры и формы этих органелл непостоянны и могут быть разными в зависимости от видов живых существ. Если описывать средние значения, то гранулярная и нитевидная митохондрия, состоящая из двух мембран, имеет размеры порядка 0,5 микромиллиметра в толщину, а длина может достигать 60 микромиллиметров.
Как уже было сказано выше, учёные долгое время пытались разобраться в вопросе, каково строение и функции митохондрий. Основные сложности были с недостаточно развитостью оборудования, потому что изучать микромир другими способами практически невозможно.
В митохондрий содержится больше, чем в клетках растений, потому что для животных преобразование энергии с эволюционной точки зрения более важно. Впрочем, объяснять подобные процессы достаточно сложно, но в клетках растений подобные функции берут на себя в основном хлоропласты.
В клетках митохондрии могут располагаться в самых разных местах, где есть потребность в АТФ. Можно сказать, что у митохондрий достаточно универсальное строение, поэтому они могут появляться в разных местах.
Функции митохондрии
Основная функция митохондрий - синтез молекул АТФ. Это своего рода энергетическая станция клетки, которая за счёт окисления различных высвобождает энергию за счёт их распада.
Главным источником энергии, т.е. соединением, используемым для распада, является Её в свою очередь организм получает из белков, углеводов и жиров. Есть два пути образования энергии, причём митохондрии используют оба. Первый из них связан с окислением пирувата в матриксе. Второй связан уже с кристами органелл и непосредственно завершает процесс энергообразования.
В целом данный механизм достаточно сложен и происходит в несколько этапов. Выстраиваются длинные единственная цель которых - энергообеспечение других клеточных процессов. Поддержание организма на клеточном уровне позволяет сохранить его жизнедеятельность в целом. Именно поэтому учёные долгое время пытались разгадать, как именно происходят данные процессы. Со временем многие вопросы были решены, особенно в этом помогло изучение ДНК и структуры остальных небольших клеток микромира. Без этого вряд ли можно было бы представить развитие данной науки в целом, а также изучение организма человека и высокоразвитых животных.