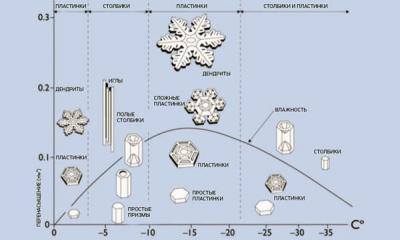
|
ТИТАН И ЕГО СПЛАВЫ |
|
Титан относится к группе тугоплавких металлов, его температура плавления равна 1668°С. Титан имеет две аллотропические модификации α и ß. Модификация α низкотемпературная и существует при нагреве 882,5°С, имеет гексагональную решетку. При темпертуре 882,5°С α-модификация переходит в ß - модификацию, имеющую объемноцентрированную кубическую рещетку. При переходе α-титана в ß - титан объем металла несколько уменьшается, а электропроводность скачкообразн возрастает. Основными достоинствами титана являются плотность (4,5 г/см 3), большая коррозионная стойкость и высокая механическая прочность. Несмотря на то, что титан химически весьма активен и легко реагирует с большим количеством элементов, он обладает высокой коррозионной стойкостью благодаря защитному действию образующейся на его поверхности прочной и плотной окисной пленки. В большинстве коррозионных сред титан и его сплавы имеют более высокую стойкость, чем кислотостойкие стали и алюминий. При введении легирующих элементов можно получать сплавы, обладающие высокой механической прочностью. Основными легирующими элементами являются Al, Sn, Мn, Cr, Мо, V. Легирующие элементы влияют на устойчивость аллотропических модификаций титана. В соответствии с влиянием легирующих элементов на аллотропические превращения титановые сплавы классифицируются по структуре следующим образом: 1) а-титановые сплавы, структура которых состоит из α-фазы (например, сплав ВТ5-1); 2) α+ß - сплавы, в структуре которых присутствуют обе фазы (ВТЗ-1, ВТ6); 3) ß - сплавы, структура которых состоит из механически стабильной ß - фазы (ВТ15); двухфазные (α+ß)-сплавы и ß - сплавы в отличие от α-сплавов упрочняются термической обработкой. Сплавы титана обладают не только более высокой механической прочностью, но и большей коррозионной стойкостью, чем чистый титан. Титан и его сплавы хорошо поддаются горячей и холодной обработке давлением, хорошо свариваются в инертной среде, но обладают низкими антифрикционными свойствами и, сравнительно со сталью, хуже обрабатываются резанием. Сплавы титана широко применяют в авиационной и ракетной технике, в химической промышленности, цветной металлургии и других отраслях, где использование титановых сплавов определяется их ценными антикоррозионными свойствами. Так, титановые теплообменники, работающие в азотной кислоте, имеют скорость коррозии в 60 раз меньшую, чем аналогичные теплообменники из нержавеющей стали. Из титана изготавливают оборудование для хлорной промышленности, гребные винты и т.п. |
Титан (Ti) (Titanium) - химический элемент с порядковым номером 22 в периодической системе элементов Д.И. Менделеева, атомный вес 47, 88, легкий серебристо-белый металл. Плотность 4, 51 г/с м³, tпл.=1668+ (-)5°С, tкип.=3260°С.
По плотности и удельной теплоемкости титан занимает промежуточное место между двумя основными конструкционными металлами: алюминием и железом. Стоит также отметить, что его механическая прочность примерно вдвое больше, чем чистого железа, и почти в шесть раз выше, чем алюминия. Но титан может активно поглощать кислород, азот и водород, которые резко снижают пластические свойства металла. С углеродом титан образует тугоплавкие карбиды, обладающие высокой твердостью.
Титан обладает низкой теплопроводностью, которая в 13 раз меньше теплопроводности алюминия и в 4 раза - железа. Коэффициент термического расширения при комнатной температуре сравнительно мал, с повышением температуры он возрастает.
Модули упругости титана невелики и обнаруживают существенную анизотропию. С повышением температуры до 350°С модули упругости уменьшаются почти по линейному закону. Небольшое значение модулей упругости титана - существенный его недостаток, т.к. в некоторых случаях для получения достаточно жестких конструкций приходится применять большие сечения изделий по сравнению с теми, которые следуют из условий прочности.
Титан имеет довольно высокое удельное электросопротивлеиие, которое в зависимости от содержания примесей колеблется в пределах от 42·10-8 до 80·10-6 Ом·см. При температурах ниже 0, 45 К он становится сверхпроводником.
Титан - парамагнитный металл. У парамагнитных веществ магнитная восприимчивость при нагревании обычно уменьшается. Титан составляет исключение из этого правила - его восприимчивость существенно увеличивается с температурой.
Для технического титана марок ВТ-00 и ВТ1-0 плотность приблизительно 4, 32 г/с м³. Титан и титановые сплавы сочетают легкость, прочность, высокую коррозийную стойкость, низкий коэффициент теплового расширения, возможность работы в широком диапозоне температур (от -290°С до 600°С).
Металл обладает рядом полезных свойств, делающих его одним из основных материалов в отдельных отраслях промышленности. Титановый прокат используется в ракетостроение и авиастроение, химической промышленности, судостроение, машиностроение
Так например, титановый
лист и титановый
пруток применяется
при создании корпусов атомных подводных
лодок;
титановые
трубы используются
в химической промышленности вследствие
их высоких антикоррозионных характеристик
и химической инертности к реактивам;
титановая
проволока используется
как присадочная проволока для создания
каркасов, форм, корпусов изтитановых
сплавов стратегического
назначения.
Титановая проволока часто используется в медицинской промышленности, в частности стоматологии. К полезным свойствам продукции из титанового проката можно отнести высокую механическую прочность, коррозионную стойкость (стоек во многих химически активных средах), жаропрочность (t пл = 1668 °С), а также малую плотность (4, 505 г/см 3). Основные физические и химические свойства титана можно посмотреть в данной таблице. Но титан имеет и свои недостатки. Одним из основных недостатков является высокая стоимость производства. Плавка титана может осуществляться только в вакууме или среде инертных газов, т.к. данный металл активно взаимодействует (особенно в жидком состоянии) со всеми газами, составляющими атмосферу. Также титановая продукция имеет плохие антифрикционные свойства, высокую склонность к водородной хрупкости и солевой коррозии, плохую обрабатываемость резанием и свариваемость.
Основой производства технического титана и его сплавов служит титановая губка, получаемая магниетермическим методом. Титановая губка - пористое серое вещество с насыпной массой 1, 5-2, 0 г/см 3 и очень высокой вязкостью.
В зависимости от содержания примесей технический титан разделяют на несколько сортов:GR1 (самый чистый титан),GR2 (более загрязненный).
Сплавы титана
По использованию в качестве конструкционного материала титан находится на 4-ом месте, уступая лишь Al, Fe и Mg. Алюминиды титана являются очень стойкими к окислению и жаропрочными, что в свою очередь определило их использование в авиации и автомобилестроении в качестве конструкционных материалов. Биологическая безвредность титана делает его превосходным материалом для пищевой промышленности и восстановительной хирургии.
Титан и его сплавы нашли широкое применеие в технике ввиду своей высокой мехнической прочности, которая сохраняется при высоких температурах, коррозионной стойкости, жаропрочности, удельной прочности, малой плотности и прочих полезных свойств. Высокая стоимость титана и его сплавов во многих случаях компенсируется их большей работоспособностью, а в некоторых случаях они являются единственным материалом, из которого можно изготовить оборудование или конструкции, способные работать в данных конкретных условиях.
Титановые сплавы играют большую роль в авиационной технике, где стремятся получить наиболее легкую конструкцию в сочетании с необходимой прочностью. Титан легок по сравнению с другими металлами, но в то же время может работать при высоких температурах (см. рис.2). Из титановых сплавов изготовляют обшивку, детали крепления, силовой набор, детали шасси, различные агрегаты. Также данные материалы применяются в конструкциях авиационных реактивных двигателей. Это позволяет уменьшить их массу на 10-25%. Из титановых сплавов производят диски и лопатки компрессора, детали воздухозаборника и направляющего аппарата, крепеж.
Также титан и его сплавы используют в ракетостроении. Ввиду кратковременной работы двигателей и быстрого прохождения плотных слоев атмосферы в ракетостроении в значительной мере снимаются проблемы усталостной прочности, статической выносливости и отчасти ползучести.
Технический титан из-за недостаточно высокой теплопрочности не пригоден для применення в авиации, но благодаря исключительно высокому сопротивлению коррозии в ряде случаев незаменим в химической промышленности и судостроении. Так его применяют при изготовлении компрессоров и насосов для перекачки таких агрессивных сред, как серная и соляная кислота и их соли, трубопроводов, запорной арматуры, автоклав, различного рода емкостей, фильтров и т. п. Только титан обладает коррозионной стойкостью в таких средах, как влажный хлор, водные и кислые растворы хлора, поэтому из данного металла изготовляют оборудование для хлорной промышленности. Из титана делают теплообменникн, работающие в коррозионно активных средах, например в азотной кислоте (не дымящей). В судостоении титан используется для изготовления гребных винтов, обшивки морских судов, подводных лодок, торпед и т.д. На титан и его сплавы не налипают ракушки, которые резко повышают сопротивление судна при его движении.
Титановые сплавы перспективны для использования во многих других применениях, но их распространение в технике сдерживается высокой стоимостью и дефицитностью титана.
Соединения титана также получили широкое применение в различных отраслях промышленности. Карбид титана обладает высокой твердостью и применяется в производстве режущих инструментов и абразивных материалов. Белый диоксид титана (TiO2) используется в красках (например, титановые белила), а также при производстве бумаги и пластика. Титанорганические соединения (напр. тетрабутоксититан) применяются в качестве катализатора и отвердителя в химической и лакокрасочной промышленности. Неорганические соединения титана применяются в химической электронной, стекловолоконной промышленности в качестве добавки. Диборид титана - важный компонент сверхтвердых материалов для обработки металлов. Нитрид титана применяется для покрытия инструментов
В настоящее время известно довольно большое разнообразие титановых сплавов, отличающихся по химическому составу, механическим и технологическим свойствам. Наиболее употребляемые легирующие элементы в титановых сплавах: алюминий, ванадий, молибден, марганец, хром, кремний, олово, цирконий, железо.
Титановый сплав ВТ5 содержит помимо титана 5% алюминия. Он отличается более высокими прочностными свойствами по сравнению с титаном, но его технологичность невелика. Сплав куется, прокатывается, штампуется и хорошо сваривается.
Из титана (сплава) ВТ5 получают титановые прутки, титановая проволока и титановые трубы. Его применяют при изготовлении деталей, работающих при температуре до 400 °С.
Сплав титана ВТ5-1 помимо 5% алюминия содержит 2-3% олова. Олово улучшает его технологические свойства. Изтитанового сплава ВТ5-1 изготовляют все виды полуфабрикатов, получаемых обработкой давлением: титановые листы, плиты, поковки, штамповки, профили, титановые трубы и титановая проволока. Он предназначен для изготовления изделий, работающих в широком интервале температур: от криогенных до 450 °С.
Титановые сплавы ОТ4 и ОТ4-1 помимо титана содержат алюминий и марганец. Они обладают высокой технологической пластичностью (хорошо деформируются в горячем и холодном состоянии) и хорошо свариваются всеми видами сварки. Титан данных марок идеет в основном на изготовление титановых листов, лент и полос, а также изготовляются титановые прутки, поковки, профили и титановые трубы. Из титановых сплавов ОТ4 иОТ4-1 изготовляют с применением сварки, штамповки и гибки детали, работающие до температуры 350 °С. Данные сплавы имеют недостатки: 1) сравнительно невысокая прочность и жаропрочность; 2) большая склонность к водородной хрупкости. В сплаве ПТ3В марганец заменяется на ванадий.
Титановый сплав ВТ20 разрабатывали как более прочный листовой сплав по сравнению с ВТ5-1. Упрочнение сплаваВТ20 обусловлено его легированием, помимо алюминия, цирконием и небольшими количествами молибдена и ванадия. Технологическая пластичность сплава ВТ20 невысока из-за большого содержания алюминия. Титан ВТ20 отличается высокой жаропрочностью. Он хорошо сваривается, прочность сварного соединения равна прочности основного металла. Сплав предназначен для изготовления изделий, работающих длительное время при температурах до 500 °С.
Титановый сплав ВТ3-1 относится к системе Ti - Al - Cr - Mo - Fe - Si. Он обычно подвергается изотермическому отжигу. Такой отжиг обеспечивает наиболее высокую термическую стабильность и максимальную пластичность. СплавВТ3-1 относится к числу наиболее освоенных в производстве сплавов. Он предназначен для длительной работы при 400 - 450 °С; это жаропрочный сплав с довольно высокой длительной прочностью. Из него поставляют титановые прутки, профили, плиты, поковки, штамповки.
Титан и его сплавы
Плавится титан при температуре 1660°С, аллотропичен, вредные примеси N, C, O, H. Пленка TiO2 защищает титан от окисления, коррозии в любой воде, некоторых кислотах. Он плавится, льется, сваривается в среде аргона, подвергается ОМД. Из титана изготавливают лист, трубы, профиль, проволоку. Сплавы его с Fe, Al, Mn, Cr, Sn, V, Si, Ga, Ge, La, Nb, Ta, Zr, W, Mo, Co, Si, имеют повышенную прочность, жаропрочность, коррозионную стойкость.Титановые сплавы термообрабатываются.
Титановые сплавы деформируются, льются, изготавливаются из порошков, закаливаются, отпускаются, хорошо мехобрабатываются.
Деформируемые сплавы титана:
− ά – сплавы: ВТ5, ВТ-5-1, ОТ-4;
− ά – β сплавы: ВТ-6, ВТ14, ВТ8; ВТ15
Литейные сплавы: ВТ5Л, ВТ6Л, ВТ14Л, ВТ3-1Л
Порошковые сплавы титана получают из порошков прессованием, они прочны, пластичны.
Из титановых сплавов изготавливают обшивку самолетов, морских судов, подводных лодок, корпуса ракет, двигателей, деталей турбин, компрессоров, гребные винты, баллоны для сжиженных газов, емкости для химических средств и много других изделий. Титановые сплавы можно подвергать, отжигу, закалке, старению и ХТО. Отжиг α – сплавов проводят при 800 – 850 0С, а α + β – сплавов – при 750 -800 0С. Вакуумный отжиг позволяет уменьшить содержание водорода, что приводит к повышению ударной вязкости, уменьшению разрушений и растрес- кивания.
При высокой концентрации легирующего элемента и закалке возникает мартенситная α׀׀ – фаза с ромбической решеткой и ω – фаза с гексагональной структурой. В процессе старения закаленных сплавов происходит их упрочнение, обусловленное распадом α׀׀ и β – фаз. Деформируемые сплавы титана хорошо обрабатываются давлением в горячем состоянии, свариваются, обладают высокой сопротивляемости коррозии.
Характерные особенности титана – малая плотность 4,51 кг/дм3 , высокая прочность, которая сохраняется до 6000С, коррозионная стойкость. Они определяют область его применения. Титановые сплавы сочетают высокую прочность (σВ= 800-1500 МПа) с хорошей пластичностью (δ= 12- 25%), относительно хорошую жаропрочность до 600- 7000С, высокую коррозионную стойкость во многих агрессивных средах кроме HCL, HF. α- титановые сплавы не стареют и используются в криогенных установках до гелиевых температур (-2720С). Одним из недостатков титановых сплавов является их плохая обрабатываемость режущим инструментом.
Титан. Изобретение титана. Титан и его сплавы.
Первооткрывателем титана считается 28-летний английский монах Уильям Грегор. В 1790 г., проводя минералогические изыскания в своем приходе, он обратил внимание на распространенность и необычные свойства черного песка в долине Менакэна на юго-западе Англии и принялся его исследовать. В песке священник обнаружил крупицы черного блестящего минерала, притягивающегося обыкновенным магнитом. Полученный в 1925 г. Ван Аркелем и де Буром иодидным методом чистейший титан оказался пластичным и технологичным металлом со многими ценными свойствами, которые привлекли к нему внимание широкого круга конструкторов и инженеров. В 1940 г. Кролль предложил магниетермический способ извлечения титана из руд, который является основным и в настоящее время. В 1947 г. были выпущены первые 45 кг технически чистого титана.
В периодической системе элементов Менделеева титан имеет порядковый номер 22. Атомная масса природного титана, вычисленная по результатам исследований его изотопов, составляет 47,926. Итак, ядро нейтрального атома титана содержит 22 протона. Количество же нейтронов, т. е. нейтральных незаряженных частиц, различно: чаще 26, но может колебаться от 24 до 28. Поэтому и число изотопов титана различно. Всего сейчас известно 13 изотопов элемента № 22. Природный титан состоит из смеси пяти стабильных изотопов, наиболее широко представлен титан-48, его доля в природных рудах 73,99%. Титан и другие элементы подгруппы IVВ очень близки по свойствам к элементам подгруппы IIIВ (группы скандия), хотя и отличаются от последних способностью проявлять большую валентность. Сходство титана со скандием, иттрием, а также с элементами подгруппы VВ – ванадием и ниобием выражается и в том, что в природных минералах титан часто встречается вместе с этими элементами. С одновалентными галогенами (фтором, бромом, хлором и йодом) он может образовывать ди- три- и, тетрасоединения, с серой и элементами ее группы (селеном, теллуром) – моно- и дисульфиды, с кислородом – оксиды, диоксиды и триоксиды.
Титан образует также соединения с водородом (гидриды), азотом (нитриды), углеродом (карбиды), фосфором (фосфиды), мышьяком (арсиды), а также соединения со многими металлами – интерметаллиды. Образует титан не только простые, но и многочисленные комплексные соединения, известно немало его соединений с органическими веществами. Как видно из перечня соединений, в которых может участвовать титан, он химически весьма активен. И в то же время титан является одним из немногих металлов с исключительно высокой коррозионной стойкостью: он практически вечен в атмосфере воздуха, в холодной и кипящей воде, весьма стоек в морской воде, в растворах многих солей, неорганических и органических кислотах. По своей коррозионной стойкости в морской воде он превосходит все металлы, за исключением благородных – золота, платины и т. п., большинство видов нержавеющей стали, никелевые, медные и другие сплавы. В воде, во многих агрессивных средах чистый титан не подвержен коррозии. Противостоит титан и эрозионной коррозии, происходящей в результате сочетания химического и механического воздействия на металл. В этом отношении он не уступает лучшим маркам нержавеющих сталей, сплавам на основе меди и другим конструкционным материалам. Хорошо противостоит титан и усталостной коррозии, проявляющейся часто в виде нарушений целостности и прочности металла (растрескивание, локальные очаги коррозии и т. п.). Поведение титана во многих агрессивных средах, в таких, как азотная, соляная, серная, «царская водка» и другие кислоты и щелочи, вызывает удивление и восхищение этим металлом.
Титан весьма тугоплавкий металл. Долгое время считалось, что он плавится при 1800° С, однако в середине 50-х гг. английские ученые Диардорф и Хейс установили температуру плавления для чистого элементарного титана. Она составила 1668±3° С. По своей тугоплавкости титан уступает лишь таким металлам, как вольфрам, тантал, ниобий, рений, молибден, платиноиды, цирконий, а среди основных конструкционных металлов он стоит на первом месте. Важнейшей особенностью титана как металла являются его уникальные физико-химические свойства: низкая плотность, высокая прочность, твердость и др. Главное же, что эти свойства не меняются существенно при высоких температурах.
Титан – легкий металл, его плотность при 0° С составляет всего 4,517 г/см8, а при 100° С – 4,506 г/см3. Титан относится к группе металлов с удельной массой менее 5 г/см3. Сюда входят все щелочные металлы (натрий, кадий, литий, рубидий, цезий) с удельной массой 0,9–1,5 г/см3, магний (1,7 г/см3), алюминий (2,7 г/см3) и др. Титан более чем в 1,5 раза тяжелее алюминия, и в этом он, конечно, ему проигрывает, но зато в 1,5 раза легче железа (7,8 г/см3). Однако, занимая по удельной плотности промежуточное положение между алюминием и железом, титан по своим механическим свойствам во много раз их превосходит.). Титан обладает значительной твердостью: он в 12 раз тверже алюминия, в 4 раза–железа и меди. Еще одна важная характеристика металла – предел текучести. Чем он выше тем лучше детали из этого металла сопротивляются эксплуатационным нагрузкам. Предел текучести у титана почти в 18 раз выше, чем у алюминия. Удельная прочность сплавов титана может быть повышена в 1,5–2 раза. Его высокие механические свойства хорошо сохраняются при температурах вплоть до нескольких сот градусов. Чистый титан пригоден для любых видов обработки в горячем и холодном состоянии: его можно ковать, как железо, вытягивать и даже делать из него проволоку, прокатывать в листы, ленты, в фольгу толщиной до 0,01 мм.
В отличие от большинства металлов титан обладает значительным электрическим сопротивлением: если электропроводность серебра принять за 100, то электропроводность меди равна 94, алюминия – 60, железа и платины –15, а титана–всего 3,8. Титан – парамагнитный металл, он не намагничивается, как железо, в магнитном поле, но и не выталкивается из него, как медь. Его магнитная восприимчивость очень слаба, это свойство можно использовать при строительстве. Титан обладает сравнительно низкой теплопроводностью, всего 22,07 Вт/(мК), что приблизительно в 3 раза ниже теплопроводности железа, в 7 раз–магния, в 17–20 раз–алюминия и меди. Соответственно и коэффициент линейного термического расширения у титана ниже, чем у других конструкционных материалов: при 20 С он в 1,5 раза ниже чем у железа, в 2 - у меди и почти в 3 - у алюминия. Таким образом, титан – плохой проводник электричества и тепла.
Сегодня
титановые сплавы широко применяют в
авиационной технике. Титановые сплавы
в промышленном масштабе впервые были
использованы в конструкциях авиационных
реактивных двигателей. Применение
титана в конструкции реактивных
двигателей позволяет уменьшить их массу
на 10...25%. В частности, из титановых сплавов
изготавливают диски и лопатки компрессора,
детали воздухозаборника, направляющего
аппарата и крепежные изделия. Титановые
сплавы незаменимы для сверхзвуковых
самолетов. Рост скоростей полета
летательных аппаратов привел к повышению
температуры обшивки, в результате чего
алюминиевые сплавы перестали удовлетворять
требованиям, которые предъявляются
авиационной техникой сверхзвуковых
скоростей. Температура обшивки в этом
случае достигает 246...316 °С. В этих условиях
наиболее приемлемым материалом оказались
титановые сплавы. В 70-х годах существенно
возросло применение титановых сплавов
для планера гражданских самолетов. В
среднемагистральном самолете ТУ-204
общая масса деталей из титановых сплавов
составляет 2570 кг. Постепенно расширяется
применение титана в вертолетах, главным
образом, для деталей системы несущего
винта, привода, а также системы управления.
Важное место занимают титановые сплавы
в ракетостроении.
Благодаря
высокой коррозионной стойкости в морской
воде титан и его сплавы находят применение
в судостроении для изготовления гребных
винтов, обшивки морских судов, подводных
лодок, торпед и т.д. На титан и его сплавы
не налипают ракушки, которые резко
повышают сопротивление судна при его
движении. Постепенно области применения
титана расширяются. Титан и его сплавы
применяют в химической, нефтехимической,
целлюлозно-бумажной и пищевой
промышленности, цветной металлургии,
энергомашиностроении, электронике,
ядерной технике, гальванотехнике, при
производстве вооружения, для изготовления
броневых плит, хирургического инструмента,
хирургических имплантатов, опреснительных
установок, деталей гоночных автомобилей,
спортинвентаря (клюшки для гольфа,
снаряжение альпинистов), деталей ручных
часов и даже украшений. Азотирование
титана приводит к образованию на его
поверхности золотистой пленки, по
красоте не уступающей настоящему золоту.
Титан и его сплавы обладают высокой коррозионной стойкостью в атм. условиях, пресной и морской воде, растворах большинства хлоридов, гипохлоритов, двуокиси хлора и мн. солей минеральных к-т как при обычной, так и при повышенных темп-рах. Высокой коррозионной стойкостью титан и его сплавы обладают также в кислых окислит. средах (азотная и хромовая к-ты и др.) и в растворе щелочей. В неокислит, кислотах (серной, соляной) титан имеет удовлетворит. коррозионную стойкость при обычных темп-pax и концентрации к-т до 8- 10%. С повышением темп-ры, концентрации к-т и щелочей скорость коррозии титана резко возрастает. Для серной к-ты наблюдаются два максимума скорости коррозии, соответствующие 40- и 75%-ной концентрации. В 40%-ной серной к-те процесс коррозии идет с выделением водорода, такая к-та характеризуется наибольшей электропроводностью и максим, концентрацией водородных ионов. В 75%-ном растворе процесс коррозии сопровождается восстановлением серной к-ты до H3S и свободной серы, а при высоких концентрациях (80- 90 %) выделяются S02 и свободная сера. В фосфорной к-те титан относительно более стоек и сохраняет высокую коррозионную стойкость до 30%-ного раствора, с повышением концентрации скорость коррозии усиливается. Добавки окислителей (K2Cr207; HNOs; Fe+ + + ; Си + +) резко снижают скорость коррозии титана и его сплавов в соляной и серной к-тах.
Титана: α-титан - гексагональная, β-титан - кубическая...
Многих интересует немного загадочный и не до конца изученный титан - металл, свойства которого отличаются некоторой двоякостью. Металл и самый прочный, и самый хрупкий.
Самый прочный и самый хрупкий металл
Его открыли двое ученых с разницей в 6 лет - англичанин У. Грегор и немец М. Клапрот. Название титана связывают, с одной стороны, с мифическими титанами, сверхъестественными и бесстрашными, с другой стороны, с Титанией - королевой фей.
Это один из самых распространенных в природе материалов, но процесс получения чистого металла отличается особой сложностью.
22 химический элемент таблицы Д. Менделеева Titanium (Ti) относится к 4 группе 4 периода.
Цвет титана серебристо-белый с выраженным блеском. Его блики переливаются всеми цветами радуги.
Это один из тугоплавких металлов. Он плавится при температуре +1660 °С (±20°). Титан отличается парамагнитностью: он не намагничивается в магнитном поле и не выталкивается из него.
Металл характеризуется низкой плотностью и высокой прочностью. Но особенность этого материала заключается в том, что даже минимальные примеси других химических элементов кардинально изменяют его свойства. При наличии ничтожной доли других металлов титан теряет свою жаропрочность, а минимум неметаллических веществ в его составе делают сплав хрупким.
Эта особенность обуславливает наличие 2 видов материала: чистого и технического.
- Титан чистого вида используют там, где требуется очень легкое вещество, выдерживающее большие нагрузки и сверхвысокие температурные диапазоны.
- Технический материал применяется там, где ценятся такие параметры, как легкость, прочность и устойчивость к коррозии.
Вещество обладает свойством анизотропности. Это означает, что металл может изменять свои физические характеристики, исходя из приложенных усилий. На эту особенность следует обращать внимание, планируя применение материала.

Титан теряет прочность при малейшем присутствии в нем примесей других металлов
Проведенные исследования свойств титана в нормальных условиях подтверждают его инертность. Вещество не реагирует на элементы, находящиеся в окружающей атмосфере.
Изменение параметров начинается при повышении температуры до +400°С и выше. Титан вступает в реакцию с кислородом, может воспламеняться в азоте, впитывает газы.
Эти свойства затрудняют получение чистого вещества и его сплавов. Производство титана основано на применении дорогостоящей вакуумной аппаратуры.
Титан и конкуренция с другими металлами
Этот металл постоянно сравнивают с алюминием и сплавами железа. Многие химические свойства титаназначительно лучше, чем у конкурентов:
- По механической прочности титан превосходит железо в 2 раза, а алюминий в 6 раз. Прочность его увеличивается при снижении температуры, чего не отмечается у конкурентов.
Антикоррозионные характеристики титана значительно превышают показатели других металлов. - При температурах окружающей среды металл абсолютно инертен. Но при повышении температуры свыше +200°С вещество начинает поглощать водород, изменяя свои характеристики.
- При более высоких температурах титан вступает в реакции с другими химическими элементами. Он обладает высокой удельной прочностью, что в 2 раза превосходит свойства лучших сплавов железа.
- Антикоррозионные свойства титана значительно превышают показатели алюминия и нержавеющей стали.
- Вещество плохо проводит электричество. Титан имеет удельное электросопротивление в 5 раз выше, чем у железа, в 20 раз, чем у алюминия, и в 10 раз выше, чем у магния.
- Титан характеризуется низкой теплопроводностью, это обусловлено низким коэффициентом температурного расширения. Она меньше в 3 раза, чем у железа, и в 12, чем у алюминия.
Какими способами получают титан?
Материал занимает 10 место по распространению в природе. Существует около 70 минералов, содержащих титан в виде титановой кислоты или его двуокиси. Наиболее распространенные из них и содержащие высокий процент производных металла:
- ильменит;
- рутил;
- анатаз;
- перовскит;
- брукит.
Основные залежи титановых руд находятся в США, Великобритании, Японии, большие месторождения их открыты в России, Украине, Канаде, Франции, Испании, Бельгии.

Добыча титана — дорогой и трудозатратный процесс
Получение металла из них стоит очень дорого. Ученые разработали 4 способа производства титана, каждый из которых рабочий и эффективно используется в промышленности:
- Магниетермический способ. Добытое сырье, содержащее титановые примеси, перерабатывают и получают диоксид титана. Это вещество подвергается хлорированию в шахтных или солевых хлораторах при повышенном температурном режиме. Процесс очень медленный, ведется в присутствии углеродного катализатора. При этом твердый диоксид переводится в газообразное вещество — тетрахлорид титана. Полученный материал восстанавливается магнием или натрием. Сплав, образовавшийся при реакции, подвергают нагреванию в вакуумной установке до сверхвысоких температур. В результате реакции происходит испарение магния и его соединений с хлором. В конце процесса получают губкоподобный материал. Его плавят и получают титан высокого качества.
- Гидридно-кальциевый способ. Руду подвергают химической реакции и получают гидрид титана. Следующий этап — разделение вещества на составляющие. Титан и водород выделяют в процессе нагревания в вакуумных установках. По окончании процесса получают оксид кальция, который отмывают слабыми кислотами. Первые два способа относятся к промышленному производству. Они позволяют получать в кратчайшие сроки чистый титан с относительно небольшими издержками.
- Электролизный метод. Титановые соединения подвергают воздействию током большой силы. В зависимости от исходного сырья, соединения разделяются на составляющие: хлор, кислород и титан.
- Йодидный способ или рафинирование. Полученный из минералов диоксид титана обдают парами йода. В результате реакции образуется йодид титана, который нагревают до высокой температуры — +1300…+1400°С и воздействуют на него электрическим током. При этом из исходного материала выделяются составляющие: йод и титан. Металл, полученный данным способом, не имеет примесей и добавок.
Области применения
Применение титана зависит от степени его очистки от примесей. Наличие даже небольшого количества других химических элементов в составе сплава титана кардинально меняет его физико-механические характеристики.
Титан с некоторым количеством примесей называется техническим. Он имеет высокие показатели коррозийной стойкости, это легкий и очень прочный материал. От этих и других показателей зависит его применение.
- В химической промышленности из титана и его сплавов изготавливают теплообменники, различного диаметра трубы, арматуру, корпуса и детали для насосов различного назначения. Вещество незаменимо в местах, где требуются высокая прочность и стойкость к кислотам.
- На транспорте титан используют для изготовления деталей и агрегатов велосипедов, автомобилей, железнодорожных вагонов и составов. Применение материала уменьшает вес подвижных составов и автомобилей, придает легкость и прочность велосипедным деталям.
- Большое значение титан имеет в военно-морском ведомстве . Из него изготавливают детали и элементы корпусов для подводных лодок, пропеллеры для лодок и вертолетов.
- В строительной промышленности применяется сплав цинк-титан. Он используется как отделочный материал для фасадов и кровель. Этот очень прочный сплав имеет важное свойство: из него можно изготавливать архитектурные детали самой фантастической конфигурации. Он может принимать любую форму.
- В последнее десятилетие титан широко применяют в нефтедобывающей отрасли . Сплавы его применяют при изготовлении оборудования для сверхглубокого бурения. Материал используется для изготовления оборудования для добычи нефти и газа на морских шельфах.

У титана очень широкая область применения
Чистый титан имеет свои области применения. Он нужен там, где необходима стойкость к высоким температурам и при этом должна сохраняться прочность металла.
Его применяют в:
- авиастроении и космической отрасли для изготовления деталей обшивки, корпусов, элементов крепления, шасси;
- медицине для протезирования и изготовления сердечных клапанов и других аппаратов;
- технике для работы в криогенной области (здесь используют свойство титана — при снижении температуры усиливается прочность металла и не утрачивается его пластичность).
В процентном соотношении использование титана для производства различных материалов выглядит так:
- на изготовление краски используется 60 %;
- пластик потребляет 20 %;
- в производстве бумаги используют 13 %;
- машиностроение потребляет 7 % получаемого титана и его сплавов.
Сырье и процесс получения титана дорогостоящие, затраты на его производство компенсируются и окупаются сроком службы изделий из этого вещества, его способностью не менять свой внешний вид за весь период эксплуатации.
НАПИШИТЕ НАМ СЕЙЧАС!
ЖМИТЕ НА КНОПКУ В ПРАВОМ НИЖНЕМ УГЛУ ЭКРАНА, ПИШИТЕ И ПОЛУЧИТЕ ЕЩЕ ЛУЧШУЮ ЦЕНУ!
Компания «ПерфектМеталл» закупает, наряду с другими металлами, лом титана. Любые пункты приема металлолома компании примут у вас титан, изделия из сплавов титана, титановую стружку и т.п. Откуда титан попадает в пункты сдачи металлолома? Все очень просто, этот металл нашел очень широкое применение как в промышленных целях, так и в быту человека. Сегодня этот металл используется при строительстве космических и военных ракет, много его используется и в самолетостроении. Из титана строят прочные и легкие морские суда. Химическая промышленность, ювелирное дело, не говоря уже об очень широком применении титана в медицинской промышленности. И все это из за того, что титан и его сплавы обладают рядом уникальных свойств.
Титан – описание и свойства
Земная кора, как известно, насыщенна многочисленным рядом химических элементов. Среди часто встречающихся среди них — титан. Можно сказать, что он находится на 10-м месте ТОПа самых распространенных хим элементов Земли. Титан - металл серебристо-белого цвета, стоек ко многим агрессивным средам, не подвержен окислению в ряде мощнейших кислот, исключениями являются лишь плавиковая, ортофосфорная серная кислота в высокой концентрации. Титан в чистом виде относительно молод, его получили лишь в 1925 году.

Пленка оксида, которая покрывает титан в чистом виде, служит весьма надежной защитой этого металла от коррозии. Ценится титан и за его низкую теплопроводность, для сравнения — титан в 13 раз хуже проводит тепло чем алюминий, а вот с проводимостью электричества обратная картина — титан обладает гораздо большим сопротивлением. Все же самой главная отличительная черта титана — его колоссальная прочность. Опять же если сравнить ее теперь с чистым железом, то титан в два раза превышает его прочность!
Сплавы титана
Сплавы из титана обладают так же выдающимися свойствами, среди которых на первом месте, как вы уже могли догадаться — прочность. Как конструкционный материал, титан уступает в прочности лишь бериллиевым сплавам. Однако неоспоримым преимуществом сплавов титана является их высокая стойкость к истиранию, износу и в то же время достаточная пластичность.

Титановые сплавы устойчивы к воздействию целого ряда активных кислот, солей, гидроксидов. Эти сплавы не боятся и высокотемпературных воздействий, именно поэтому из титана и его сплавов изготавливают турбины реактивных двигателей, да и вообще широко используются в ракетостроении и авиационной промышленности.
Где используется титан
Титан используется там, где необходим очень прочный материал, обладающий максимальной стойкостью к различным видам негативного воздействия. Например, в химической промышленности титановые сплавы применяются для производства насосов, емкостей и трубопроводов для транспортировки агрессивных жидкостей. В медицине титан служит для протезирования и обладает отличной биологической совместимостью с организмом человека. Кроме того, сплав титана и никеля – нитинол – обладает “памятью”, что позволяет использовать его в ортопедической хирургии. В металлургии титан служит легирующим элементом, который вводят в состав некоторых видов стали.

Благодаря сохранению пластичности и прочности под воздействием низких температур, металл используют в криогенной технике. В авиа- и ракетостроении титан ценится за свою жаропрочность, а наиболее широкое распространение здесь получил его сплав с алюминием и ванадием: именно из него изготавливают детали для корпусов летательных аппаратов и реактивных двигателей.

В свою очередь, в судостроении титановые сплавы применяют для изготовления металлических изделий с повышенной коррозийной устойчивостью. Но, помимо промышленного использования, титан служит сырьем для создания украшений и аксессуаров, так как он хорошо поддается таким методам обработки, как полировка или анодирование. В частности, из него отливают корпуса наручных часов и ювелирные украшения.

Титан получил широкое применение в составе различных соединений. Например, диоксид титана входит в состав красок, используется в процессе производства бумаги и пластика, а нитрид титана выступает в роли защитного покрытия инструментов. Несмотря на то, что титан называют металлом будущего, на данном этапе сфера его применения серьезно ограничена высокой стоимостью получения.
Таблица 1
| Химический состав промышленных титановых сплавов. | ||||||||
| Тип сплава | Марка сплава | Химический состав, % (остальное Ti) | ||||||
| Аl | V | Mo | Mn | Cr | Si | Другие элементы | ||
| a | ВТ5 ВТ5-1 |
4,3-6,2 4,5-6,0 |
— — |
— — |
— — |
— — |
— — |
— 2-3Sn |
| Псевдо-a | ОТ4-0 ОТ4-1 ОТ4 ВТ20 ВТ18 |
0,2-1,4 1,0-2,5 3,5-5,0 6,0-7,5 7,2-8,2 |
— — — 0,8-1,8 — |
— — — 0,5-2,0 0,2-1,0 |
0,2-1,3 0,7-2,0 0,8-2,0 — — |
— — — — — |
— — — — 0,18-0,5 |
— — — 1,5-2,5Zr 0,5-1,5Nb 10-12Zr |
| a + b | ВТ6С ВТ6 ВТ8 ВТ9 ВТ3-1 ВТ14 ВТ16 ВТ22 |
5,0-6,5 5,5-7,0 6,0-7,3 5,8-7,0 5,5-7,0 4,5-6,3 1,6-3,0 4,0-5,7 |
3,5-4,5 4,2-6,0 — — — 0,9-1,9 4,0-5,0 4,0-5,5 |
— — 2,8-3,8 2,8-3,8 2,0-3,0 2,5-3,8 4,5-5,5 4,5-5,0 |
— — — — — — — — |
— — — — 1,0-2,5 — — 0,5-2,0 |
— — 0,20-0,40 0,20-0,36 0,15-0,40 — — — |
— — — 0,8-2,5Zr 0,2-0,7Fe — — 0,5-1,5Fe |
| b | ВТ15 | 2,3-3,6 | — | 6,8-8,0 | — | 9,5-11,0 | — | 1,0Zr |
Титан (Titanium),Ti,- химический элемент IV группы периодической системы элементов Д. И. Менделеева. Порядковый номер 22, атомный вес 47,90. Состоит из 5 устойчивых изотопов; получены также искусственно радиоактивные изотопы.
В 1791 году английский химик У. Грегор нашёл в песке из местечка Менакан (Англия, Корнуолл) новую «землю», названную им менакановой. В 1795 году немецкий химик М. Клаирот открыл в минерале рутиле неизвестную еще землю, металл которой он назвал Титан [в греч. мифологии титаны - дети Урана (Неба) и Геи (Земли)]. В 1797 году Клапрот доказал тождество этой земли с открытой У. Грегором. Чистый титан выделен в 1910 году американским химиком Хантером посредством восстановления четырёххлористого титана натрием в железной бомбе.
Нахождение в природе
Титан относится к числу наиболее распространённых в природе элементов, его содержание в земной коре составляет 0,6% (весовых). Встречается главным образом в виде двуокиси TiO 2 или её соединений - титанатов. Известно свыше 60 минералов, в состав которых входит титан Он содержится также в почве, в животных и растительных организмах.Ильменит FeTiO 3 ирутил TiO 2 служат основным сырьём для получения титана. В качестве источника титана приобретают значение шлаки от плавкититано-магнетитов и ильменита.
Физические и химические свойства
Титан существует в двух состояниях: аморфный - темносерый порошок, плотность 3,392-3,395г/см 3 , и кристаллический, плотность 4,5 г/см 3 . Для кристаллического титана известны две модификации с точкой перехода при 885° (ниже 885° устойчивая гексагональная форма, выше - кубическая); t° пл около 1680°;t° кип выше 3000°. Титан активно поглощает газы (водород, кислород, азот), которые делают его очень хрупким. Технический металл поддаётся горячей обработке давлением. Совершенно чистый металл может быть прокатан на холоду. На воздухе при обыкновенной температуре титан не изменяется, при накаливании образует смесь окисиTi 2 O 3 и нитридаTiN. В токе кислорода при красном калении окисляется до двуокисиTiO 2 . При высоких температурах реагирует с углеродом, кремнием, фосфором, серой и др. Устойчив к морской воде, азотной кислоте, влажному хлору, органическим кислотам и сильным щелочам. Растворяется в серной, соляной и плавиковой кислотах, лучше всего - в смесиHFиHNO 3 . Добавление к кислотам окислителя предохраняет металл от коррозии при комнатной температуре. Галогениды четырёхвалентного титана, за исключениемTiCl 4 - кристаллические тела, легкоплавкие и летучие в водном растворе гидрализованы, склонны к образованию комплексных соединений, из которых в технологии и аналитической практике имеет значение фтортитанат калияK 2 TiF 6 . Важное значение имеют карбидTiCи нитридTiN- металлоподобные вещества, отличающиеся большой твёрдостью (карбид титан тверже карборунда), тугоплавкостью (TiC,t° пл = 3140°; TiN,t° пл = 3200°) и хорошей электропроводностью.
Химический элемент №22. Титан.
Электронная формула титана имеет вид: 1s 2 |2s 2 2p 6 |3s 2 3p 6 3d 2 |4s 2 .
Порядковый номер титана в периодической системе химических элементов Д.И. Менделеева – 22. Номер элемента обозначает заряд ярда, следовательно у титана заряд ядра - +22, масса ядра – 47,87. Титан находится в четвертом периоде, в побочной подгруппе. Номер периода указывает на количество электронных слоев. Номер группы обозначает количество валентных электронов. Побочная подгруппа указывает на то, что титан относится к d-элементам.
Титан имеет два валентных электрона на s-орбитали внешнего слоя и два валентных электрона наd-орбитали предвнешнего слоя.
Квантовые числа для каждого валентного электрона:
4s4sС галогенами и водородом Ti(IV) образует соединения видаTiX 4 , имеющиеsp 3 →q 4 вид гибридизации.
Титан – металл. Является первым элементом d-группы. Наиболее устойчивым и распространенным являетсяTi +4 . Так же существуют соединения с более низкими степенями окисления –Ti 0 ,Ti -1 ,Ti +2 ,Ti +3 , но эти соединения легко окисляются воздухом, водой или другими реагентами вTi +4 . Отрыв четырех электронов требует больших затрат энергии, поэтому ионTi +4 реально не существует и соединенияTi(IV) обычно включают связи ковалентного характера.Ti(IV) в некоторых отношениях сходен с элементами –Si,Ge,SnиPb, особенно сSn.
Титан – химический элемент IV группы 4 периода периодической системы Менделеева, атомный номер 22; прочный и легкий металл серебристо-белого цвета. Существует в следующих кристаллических модификациях: α-Ti с гексагональной плотноупакованной решеткой и β-Ti с кубической объемно-центрированной упаковкой.
Титан стал известен человеку всего около 200 лет назад. История его открытия связана с именами немецкого химика Клапрота и английского исследователя-любителя Мак-Грегора. В 1825 году И. Берцелиус первым сумел выделить чистый металлический титан, однако вплоть до XX века этот металл считался редким и поэтому непригодным для практического применения.
Однако к нашему времени установлено, что по распространенности титан занимает девятое место среди других химических элементов, а его массовая доля в земной коре составляет 0,6%. Титан содержится во многих минералах, чьи запасы исчисляются сотнями тысяч тонн. Значительные месторождения титановых руд находятся на территории России, Норвегии, США, на юге Африки, а в Австралии, Бразилии, Индии расположены удобные для добычи открытые россыпи титансодержащих песков.
Титан – легкий и пластичный металл серебристо-белого цвета, температура плавления 1660±20 C, температура кипения 3260 C, плотность двух модификаций и соответственно равна α-Ti - 4,505 (20 C) и β-Ti - 4,32 (900 C) г/см3. Титан отличается высокой механической прочностью, сохраняющейся даже при высоких температурах. Имеет высокую вязкость, что при его механической обработке требует нанесения специальных покрытий на режущий инструмент.
При обычной температуре поверхность титана покрывается пассивирующей оксидной пленкой, что делает титан коррозионностойким в большинстве сред (за исключением щелочной). Титановая стружка пожароопасна, а титановая пыль – взрывоопасна.
Титан не растворяется в разбавленных растворах многих кислот и щелочей (кроме плавиковой, ортофосфорной и концентрированной серной кислот), однако в присутствии комплексообразователей легко взаимодействует даже со слабыми кислотами.
При нагревании на воздухе до температуры 1200С титан загорается, образуя оксидные фазы переменного состава. Из растворов солей титана выпадает в осадок гидроксид титана, прокаливание которого позволяет получить диоксид титана.
При нагревании титан также взаимодействует с галогенами. В частности, так получают тетрахлорид титана. В результате восстановления тетрахлорида титана алюминием, кремнием, водородом и некоторыми другими восстановителями получают трихлорид и дихлорид титана. Титан взаимодействует с бромом и иодом.
При температуре более 400С титан вступает в реакцию с азотом, образуя нитрид титана. Титан взаимодействует и с углеродом с образованием карбида титана. При нагревании титан поглощает водород, при этом образуется гидрид титана, при повторном нагревании разлагающийся с выделением водорода.
Чаще всего в качестве исходного материала для производства титана выступает диоксид титана с небольшим количеством примесей. Это может быть как титановый шлак, получаемый при переработке ильменитовых концентратов, так и рутиловый концентрат, который получают при обогащении титановых руд.
Концентрат титановых руд подвергается пирометаллургической или сернокислотной переработке. Продуктом сернокислотной обработки становится порошок диоксида титана. При использовании пирометаллургического метода руда спекается с коксом и обрабатывается хлором с получением паров тетрахлорида титана, которые затем при 850С восстанавливаются магнием.
Полученная титановая «губка» переплавляется, расплав очищается от примесей. Для рафинирования титана применяется иодидный способ или электролиз. Титановые слитки получают путем дуговой, плазменной или электроннолучевой переработки.
Большая часть производства титана поступает на нужды авиационной и ракетной промышленности, а также морского судостроения. Титан используется как легирующая добавка к качественным сталям и в качестве раскислителя.
Из него изготовляют различные детали электровакуумных приборов, компрессоры и насосы для перекачки агрессивных сред, химические реакторы, опреснительные установки и многое другое оборудование и конструкции. Благодаря своей биологической безвредности титан является превосходным материалом для применения в пищевой и медицинской промышленности.